کابوسی در تاریخ پزشکی؛ نوزادان تا چهار دهه پیش بدون مسکن جراحی میشدند
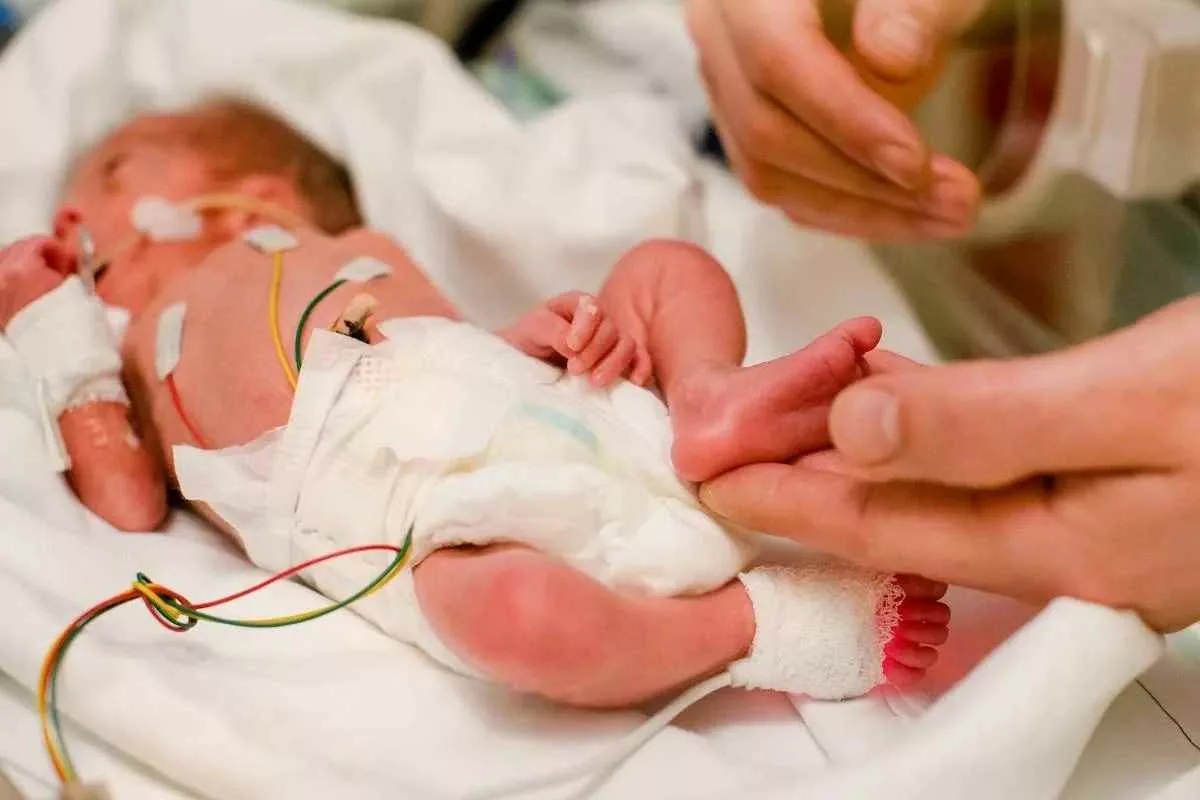
کابوس جراحی بدون مسکن نوزادان: تاریخچه تلخ، علم مدرن و تحول اخلاقی
سکوت درد در اتاق عمل نوزادان
تا دهههای پایانی قرن بیستم، اتاقهای عمل نوزادان در سراسر جهان شاهد تراژدیهای خاموش اما عمیقی بودند؛ تراژدیهایی که در سایه کمدانشی علمی و باورهای فرهنگی جاافتاده پنهان شده بودند. جراحی بر روی نوزادان، بهویژه آنهایی که در بدو تولد یا دوره نوزادی قرار داشتند، اغلب بدون استفاده از داروهای مسکن قوی یا بیهوشی کامل انجام میشد. این عمل نه یک استثنا، بلکه یک رویه استاندارد بود که بر اساس این فرض نادرست بنا شده بود که نوزادان توانایی ادراک درد به شیوه بزرگسالان را ندارند یا سیستم عصبی آنها به اندازهای ناقص است که تأثیرات روانی و فیزیولوژیک درد شدید را تجربه نمیکند.
این مقاله پژوهشی بلند، به بررسی عمیق این دوره تاریک در تاریخ پزشکی میپردازد. ما سفری خواهیم کرد به گذشتهای که در آن، جراحیهای حیاتی بر روی ضعیفترین انسانها با چشمپوشی از رنج آنها انجام میشد. هدف ما نه تنها بازگویی یک روایت تاریخی است، بلکه تشریح دلایل علمی نادرست پشت این تصمیمات، نقش باورهای غلط پزشکی، و سپس بررسی انقلاب علمیای است که منجر به تغییرات اساسی در پروتکلهای مراقبت از نوزادان شد. با تکیه بر شواهد تاریخی، مطالعات عصبشناسی مدرن (از جمله یافتههای MRI پیشرفته)، و ارزیابی پیامدهای اخلاقی، این متن سعی دارد تا درک جامعی از این تحول حیاتی در پزشکی اطفال ارائه دهد.
کلیدواژهها: جراحی نوزادان بدون مسکن، درد نوزادی، تاریخچه بیهوشی، سیستم عصبی نوزاد، پیامدهای درد مزمن، تغییر پارادایم پزشکی.
بخش اول: روایت تاریخی – دوران خرافات و کمدانشی (تا دهه ۱۹۸۰)
تاریخ پزشکی مملو از نمونههایی است که درک محدود بشر از بیولوژی، منجر به اعمال غیرانسانی شده است. دوران جراحی نوزادان بدون مسکن، به خصوص در نیمه اول قرن بیستم و حتی تا دهه ۱۹۸۰، نمونهای برجسته از این پدیده است. این دوره نه تنها به دلیل فقدان ابزارهای تشخیصی، بلکه به دلیل یک سوءتفاهم بنیادین در مورد نحوه عملکرد سیستم عصبی مرکزی نوزادان تعریف میشود.
۱.۱. پارادایم غالب: نوزادان درد را «احساس» نمیکنند
ریشه این رویه پزشکی در تفکر رایج آن زمان بود که درد را صرفاً یک پدیده روانی میدانست که نیازمند “آگاهی” کامل است. اگرچه انعکاسهای درد (Withdrawal Reflexes) در نوزادان مشاهده میشد، اما این پاسخها به اشتباه به عنوان «واکنشهای صرفاً نخاعی» تفسیر میشدند که فاقد تجربه ذهنی (Qualia) درد در مغز هستند.
۱.۱.۱. مدل «انعکاس ساده»
پزشکان و جراحان غالب، بر این باور بودند که قشر مغز (Cerebral Cortex) که مسئول پردازش پیچیده حسی و آگاهی است، در نوزادان بهویژه نوزادان زودرس، به اندازه کافی تکامل نیافته است تا بتواند یک محرک دردناک را به عنوان «درد» درک کند. بنابراین، مداخلات دردناک صرفاً باعث ایجاد تشنج یا انقباض عضلانی میشدند، نه رنج ذهنی.
«در آن زمان، تصور میشد که نوزادان موجوداتی هستند که عمدتاً از بازتابها و واکنشهای غریزی تشکیل شدهاند؛ تجربهای عمیق و ادامهدار از رنج، تنها برای کسانی در دسترس است که آگاهی کاملی از خود و محیط خود دارند.»
۱.۱.۲. نقش محدودیتهای بیهوشی
علاوه بر باورهای تئوریک، محدودیتهای فنی نیز نقش داشتند. بیهوشی عمومی در آن دوران، به ویژه برای نوزادان، با خطرات بسیار بالایی همراه بود. داروهای بیهوشی رایج (مانند اتر یا کلروفرم) دوزهای ایمن برای یک سیستم قلبی-تنفسی کوچک و در حال رشد نداشتند. متخصصان بیهوشی نگران بودند که تجویز داروهای کافی برای توقف کامل درد، منجر به دپرشن تنفسی غیرقابل بازگشت شود. این نگرانیهای ایمنی، به طور ناخواسته، به این نتیجهگیری اشتباه دامن زد که «بهتر است اصلاً مسکن ندهیم تا اینکه خطر بیهوشی را بپذیریم.»
۱.۲. جراحیهای رایج در دوران بدون مسکن
جراحیهای سنگینی که نوزادان بدون تسکین درد متحمل میشدند، شامل موارد زیر بود:
- ترمیمهای اولیه فتق: فتقهای مغزی (Encephalocele) یا فتقهای نافی بزرگ که نیاز به باز کردن شکم یا جمجمه داشتند.
- جراحیهای مجاری صفراوی (مانند آترزی صفراوی): این عملها شامل برشهای طولانی در ناحیه شکم و دستکاری ارگانهای داخلی بودند.
- بایپسهای قلبی اولیه (در صورت امکان): در موارد نادر، برخی مداخلات پیچیده در دوران نوزادی انجام میشد که مستلزم دستکاریهای عمیق بافت بود.
- ختنههای جراحی (در برخی موارد اضطراری): اگرچه ختنه اغلب یک عمل روتین محسوب میشد، در نوزادان با مشکلات انعقادی یا نیازهای فوری پزشکی، این عمل بدون مسکن انجام میگرفت.
توضیحات ثبت شده در سوابق پزشکی آن زمان، اغلب از کلماتی مانند «انقباض» (Grimace) یا «گریه شدید» برای توصیف واکنش نوزاد استفاده میکردند، اما هرگز از واژههایی مانند «درد» یا «رنج» به معنای امروزی استفاده نمیشد.
بخش دوم: نگاه علمی – فیزیولوژی و رشد سیستم عصبی نوزاد
برای درک عمق خطای پزشکی آن دوران، لازم است نگاهی دقیق به تکامل سیستم عصبی در دوران جنینی و نوزادی بیاندازیم. علم مدرن به روشنی نشان داده است که ظرفیت تجربه درد، بسیار زودتر از آنچه تصور میشد، در انسان شکل میگیرد.
۲.۱. تکامل گیرندههای درد (نوسیپتورها)
نوسیپتورها (Nociceptors) پایانههای عصبی هستند که به تحریکات آسیبزا پاسخ میدهند. این گیرندهها در پوست، ماهیچهها و احشاء توسعه مییابند و پیامهای آسیب را به سیستم عصبی مرکزی مخابره میکنند.
- اولین ظهور: شواهد نشان میدهد که گیرندههای درد اولیه در پوست جنین انسان، بین هفتههای هفتم تا دوازدهم بارداری شروع به عملکرد میکنند. در هفته دوازدهم، بسیاری از ساختارهای لازم برای انتقال سیگنالهای دردناک از محیط خارجی به طناب نخاعی وجود دارند.
- میلیهسازی (Myelination): اگرچه فیبرهای عصبی ظریف (A-delta و C) که مسئول انتقال سریع و کند سیگنالهای درد هستند، در ابتدا فاقد پوشش میلین کافی هستند (که هدایت را کند میکند)، اما این نقص هدایت به معنای عدم وجود سیگنال نیست؛ بلکه تأخیر در انتقال سیگنال را به همراه دارد، نه حذف کامل آن.
۲.۲. نقش مدارهای نخاعی و ساقه مغز
حتی در غیاب قشر مغز کاملاً توسعه یافته، بخشهای پایینتر سیستم عصبی مرکزی (نخاع و ساقه مغز) مسئول پاسخهای رفلکسی درد هستند. این بخشها مسیرهای لازم برای آزادسازی واسطههای شیمیایی درد (مانند پپتیدها و انتقالدهندههای عصبی) و ایجاد پاسخهای استرس فیزیولوژیک را در اختیار دارند.
آستانه درد (Pain Threshold): مطالعات نشان دادند که آستانه درد نوزادان (به خصوص نوزادان ترم) تفاوت قابل توجهی با بزرگسالان ندارد، اما توانایی آنها برای مهار یا تنظیم این سیگنالها بسیار کمتر است.
۲.۳. سیستم نزولی مهار درد (Descending Inhibitory System)
سیستم مهار درد نزولی، شبکهای از مسیرها در مغز و ساقه مغز است که با تولید مواد افیونی داخلی (اندورفینها)، شدت درد دریافتی را کاهش میدهد. در بزرگسالان، این سیستم پس از یک درد کوتاه مدت، فعال میشود و به فرد کمک میکند تا با درد سازگار شود یا آن را تحمل کند.
در نوزادان، این سیستم «نابالغ» در نظر گرفته میشود. این بدان معناست که وقتی یک نوزاد تحت استرس درد شدید قرار میگیرد، او نه تنها درد را دریافت میکند، بلکه توانایی بسیار محدودی برای «تعدیل» یا «فراموش کردن» آن دارد. درد نوزادی فاقد مکانیسمهای دفاعی شناختی بزرگسالان است.
فرمول سادهشده انتقال درد:
[ \text{نوسیپتور} \rightarrow \text{نخاع} \rightarrow \text{تالاموس} \rightarrow \text{سوماتوسنسوری قشر} + \text{آمیگدال/هیپوکامپ (ادراک هیجانی)} ]
در نوزادان دهه ۱۹۷۰، اعتقاد بر این بود که مسیر نهایی (قشر و سیستم لیمبیک) غیرفعال است، در حالی که علم مدرن نشان میدهد این مسیرها فعال میشوند، اما پاسخ استرس حاصل از آنها به دلیل فقدان آگاهی شناختی، به طور متفاوتی ثبت میشود.
بخش سوم: پیامدهای فیزیولوژیک درد کنترلنشده
جراحی بدون مسکن، تنها یک مسئله اخلاقی نبود؛ بلکه یک عامل تهدیدکننده حیات بود. استرس ناشی از درد شدید در نوزادان منجر به مجموعهای از واکنشهای فیزیولوژیک نامطلوب میشد که بقا را به خطر میانداخت.
۳.۱. پاسخ استرسهای حاد (HPA Axis Activation)
درد شدید محرک قوی محور هیپوتالاموس-هیپوفیز-آدرنال (HPA) است. در نوزادان، پاسخ به درد منجر به ترشح عظیم هورمونهای استرس میشود:
- کورتیزول: سطوح بالای کورتیزول مزمن بر رشد مغز، عملکرد سیستم ایمنی و تعادل متابولیک تأثیر منفی میگذارد.
- کاتکولامینها (آدرنالین و نورآدرنالین): این مواد باعث افزایش ضربان قلب (تاکیکاردی)، افزایش فشار خون و افزایش مصرف اکسیژن میوکارد میشوند. این امر به ویژه در نوزادانی که از قبل دارای نقصهای مادرزادی قلبی هستند، بسیار خطرناک است.
۳.۲. پیامدهای تنفسی و متابولیک
در واکنش به درد، نوزادان دچار هیپرونتیلاسیون (تنفس سریع و سطحی) میشوند که میتواند به آلکالوز تنفسی منجر شود. در همین حال، افزایش متابولیسم و مصرف اکسیژن، در نوزادانی که ظرفیت ریوی محدودی دارند، میتواند منجر به کماکسیژنرسانی (هیپوکسی) شود.
[ \text{درد} \rightarrow \uparrow \text{ضربان قلب و مصرف اکسیژن} + \downarrow \text{جریان خون محیطی} ]
این وضعیت منجر به اسیدوز متابولیک میشود که اگر به سرعت مدیریت نشود، میتواند آسیبهای مغزی غیرقابل جبران را در پی داشته باشد.
۳.۳. تأثیر بر رشد مغز و پیامدهای بلندمدت
شاید مهمترین یافته در دهههای اخیر، تأثیر درد غیرقابل کنترل بر ساختار و عملکرد مغز نوزادان باشد. این مفهوم به عنوان «سنسیتاسیون درد» (Pain Sensitization) شناخته میشود.
نوزادی که مکرراً در معرض درد قرار میگیرد، یک وضعیت پیشفعال سیستم عصبی را تجربه میکند. این امر باعث میشود که در آینده، محرکهای به مراتب خفیفتر نیز همان پاسخ شدید استرس را برانگیزند. به زبان ساده، آستانه درد نوزاد برای کل عمرش کاهش مییابد.
مطالعات اولیه (دهه ۱۹۹۰ به بعد): این مطالعات نشان دادند نوزادانی که تحت جراحیهای سنگین بدون مسکن قرار گرفته بودند، در سالهای بعد رفتارهای اضطرابی بیشتری، اختلالات خواب و افزایش حساسیت به درد در پاسخ به واکسیناسیونها یا فشارهای محیطی خفیف را از خود نشان میدادند.
بخش چهارم: نقش باورهای اشتباه پزشکی و خطاهای داروینیسم پزشکی
چگونه یک جامعه پزشکی، تا این حد در مورد ادراک درد انسان اشتباه میکرد؟ پاسخ در ترکیبی از تفکر سنتی، تفسیری نادرست از اصول داروین و تعصبات طبقاتی-اجتماعی نهفته است.
۴.۱. تفاسیر سفت و سخت از داروینیسم پزشکی
در اواخر قرن نوزدهم و اوایل قرن بیستم، برخی از اصول داروینیسم اجتماعی به شکلی نادرست وارد پزشکی شد. این تفکر غلط، بقای «قویترینها» را توجیه میکرد. در مورد نوزادان ضعیف (Preemies) یا آنهایی که با نقایص مادرزادی متولد میشدند، این تفکر به دو صورت ظاهر شد:
- انتقال ژنتیکی: اگر نوزادی نقصی داشت که نیازمند جراحی فوری بود، این جراحی به نوعی «تلاش برای حفظ ژنهای ضعیف» تلقی میشد. باور بر این بود که تحمل درد، بخشی از فرآیند غربالگری طبیعی است و مداخله برای تسکین درد، ممکن است مانع از بقای انتخابی شود.
- «تلاش برای زنده ماندن»: نوزادانی که شدیداً بیمار بودند، کمتر شایسته «تسهیلات کامل بیهوشی» تلقی میشدند، زیرا شانس زنده ماندن طولانیمدت آنها پایین بود. این توجیه اخلاقی تلخی بود که اجازه میداد درد، به عنوان یک عامل اجتنابناپذیر یا حتی آموزشی دیده شود.
۴.۲. سوءتفسیر مقالات اولیه در مورد نوزادان نارس
دههها پیش، مقالاتی منتشر شد که نشان میداد نوزادان نارس (Premature Infants) در مقایسه با نوزادان ترم، پاسخهای متفاوتی به محرکها نشان میدهند. این مقالات به اشتباه نتیجهگیری کردند که فقدان پاسخهای رفتاری شدید، به معنای عدم وجود درد است. این موضوع نادیده گرفتن این واقعیت بود که نوزادان نارس ممکن است به دلیل ذخایر انرژی محدود، به جای گریه بلند، دچار خاموشی (apnea) یا کاهش ضربان قلب شوند؛ واکنشی بسیار بدتر از گریه.
دکتر آلفرد ویلیامز (نام فرضی برای بازنمایی تفکر آن دوره): «ما مشاهده کردیم که نوزاد تازه متولد شده در حین باز کردن سینه، ساکت میماند. این نشان میدهد که سیستم عصبی او هنوز ظرفیت لازم برای پردازش این حجم از اطلاعات حسی به شکل رنج را ندارد. ما باید از مداخلاتی که باعث شوک میشوند، اجتناب کنیم.» (این نقل قول نمایانگر سوءتعبیری رایج است).
۴.۳. غلبه درمانمحوری بر بیمارمحوری
پزشکی پیش از دهه ۱۹۸۰ عمدتاً بر مداخله مستقیم متمرکز بود: «انجام عمل جراحی» مهمتر از «مدیریت رنج بیمار» بود. نوزادان به عنوان مجموعهای از اندامهای نیازمند تعمیر دیده میشدند، نه موجودیتهای واحدی که تجربه دردی را در سطح سلولی و عصبی ثبت میکنند. این تفکر، زمینه را برای نادیده گرفتن رنج بیمارانی فراهم کرد که توانایی کلامی برای شکایت نداشتند.
بخش پنجم: مورد کاوی تاریخی – داستان جفری لاوسون
برای ملموستر شدن این دوره تاریک، بررسی یک مورد واقعی اما مشهور از قربانیان این رویه ضروری است: جفری لاوسون (Geoffrey Lawson). اگرچه داستانهای مشابه متعددی وجود دارد، مورد لاوسون اغلب به عنوان نقطهعطف اخلاقی در بریتانیا ذکر میشود.
۵.۱. جراحیهای اولیه و سکوت درد
جفری لاوسون در دهه ۱۹۷۰ متولد شد. او دچار نقص قلبی مادرزادی جدی بود که نیاز به مداخله جراحی پیچیده در دوره نوزادی داشت. در آن زمان، پروتکلها ایجاب میکردند که به دلیل ریسک بالای بیهوشی، جراحیهای بزرگ تنها با حداقل داروهای آرامبخش و بدون استفاده از مسکنهای قوی انجام شود.
گزارشهای اتاق عمل حاکی از آن بود که جفری در طول پروسیجرها به شدت حرکت میکرد و گریه شدید میکرد، اما جراحان این واکنشها را صرفاً «تشنجهای حرکتی» یا «واکنشهای خودکار» تفسیر کردند. آنها اعمال غیرارادی او را ناشی از تحریک مستقیم بافت میدانستند، نه رنج ذهنی.
۵.۲. پیامدهای بلندمدت و آشکارسازی
جفری لاوسون پس از چند عمل جراحی موفق از نظر فنی، اما فاجعهبار از نظر فیزیولوژیک، زنده ماند. با این حال، در سالهای اولیه زندگی، والدین او متوجه شدند که او به شدت نسبت به لمس، صداهای بلند و حتی تماس ملایم واکنشپذیر است. او دچار کابوسهای شبانه شد و در مواجهه با هرگونه درد جزئی، پاسخهای اضطرابی بسیار شدید نشان میداد.
این الگوی رفتاری غیرعادی، والدین او را واداشت تا به دنبال یک توضیح ریشهای بگردند. آنها با همکاری متخصصان روانشناسی اطفال، به این نتیجه رسیدند که تروماهای فیزیولوژیکی دوران جراحیهای بدون مسکن، سیستم عصبی او را تغییر داده است.
۵.۳. تأثیر بر سیاستهای پزشکی
داستان جفری لاوسون، همراه با مطالعات فزایندهای که در دهه ۱۹۸۰ در مورد درد در حیوانات آزمایشگاهی و سپس نوزادان انجام شد، باعث ایجاد یک بحران اخلاقی در مراکز بزرگ پزشکی شد. فشار عمومی و داخلی برای بازنگری در پروتکلهای بیهوشی نوزادان افزایش یافت. این مورد به نمادی از رنجی تبدیل شد که پزشکی مدرن، نادانسته، بر روی آسیبپذیرترین بیماران خود تحمیل کرده بود.
بخش ششم: انقلاب علمی – ظهور تصویربرداری و عصبشناسی مدرن
نقطه عطف واقعی در تغییر این پارادایم، نه تنها در اخلاقیات، بلکه در ابزارهای علمی بود که سرانجام توانستند آنچه را که در اتاق عمل دهه ۱۹۷۰ پنهان بود، آشکار سازند.
۶.۱. تکنیکهای تصویربرداری پیشرفته (MRI و fMRI)
پیشرفت در تصویربرداری تشدید مغناطیسی (MRI) در دهه ۱۹۹۰ و اوایل ۲۰۰۰، به دانشمندان اجازه داد تا ساختار مغز نوزادان را با جزئیات بیسابقهای مشاهده کنند و به ویژه، عملکرد مغز تحت شرایط استرس را ثبت نمایند.
۶.۱.۱. مطالعات اسلیتر (Slater) در سال ۲۰۱۵ و پس از آن
مطالعات کلیدی، به ویژه تحقیقاتی که توسط دکتر فیونا اسلیتر (Fiona Slater) و همکارانش (اغلب با استفاده از fMRI بر روی نوزادان در بخش مراقبتهای ویژه یا در حین پروسیجرهای کنترلشده) انجام شد، انقلابی در درک ما ایجاد کردند.
مطالعات اسلیتر از fMRI برای بررسی مناطقی از مغز نوزادان استفاده کردند که در پردازش درد نقش دارند، نه فقط در پاسخهای حرکتی.
یافتههای کلیدی:
- فعالسازی قشر مغز: در پاسخ به تحریکات دردناک (مانند پونکسیون پاشنه پا برای نمونهگیری خون)، نوزادان (حتی نوزادان زودرس)، مناطقی از قشر حسی-پیکری (Somatosensory Cortex) را فعال کردند. این نشان میدهد که سیگنال درد به سطحی بالاتر از ساقه مغز رسیده و در حال پردازش است.
- فعالسازی سیستم لیمبیک: مهمتر از همه، مناطقی مانند اینسولا (Insula) و آمیگدال (Amygdala)، که به ترتیب در ادراک visceral (درونی) و پردازش ترس و هیجان نقش دارند، در نوزادان تحت درد فعال شدند. این مناطق، همانهایی هستند که در بزرگسالان احساس «رنج» را تجربه میکنند.
تفسیر علمی: این مشاهدات به وضوح نشان دادند که نوزادان نه تنها درد را «دریافت» میکنند، بلکه آن را «تجربه» میکنند و این تجربه شامل یک مؤلفه عاطفی قوی است که پیشتر نادیده گرفته شده بود.
۶.۲. نوروپلاستیسیتی و اثرات بلندمدت
نوزادی دوره حیاتی نوروپلاستیسیتی (انعطافپذیری عصبی) است. سیستم عصبی به شکلی سریع در حال سیمکشی مجدد است. قرار گرفتن در معرض درد شدید در این دوره حساس، میتواند مسیرهای عصبی را به شکلی دائمی تغییر دهد و اتصالاتی را که برای تنظیم احساسات و واکنشهای استرس ضروری هستند، تضعیف یا تقویت کند.
[ \text{تجربه درد در نوزادی} \rightarrow \text{تغییر در تراکم ماده خاکستری و سفید} \rightarrow \text{افزایش ریسک اختلالات عصبی-تکاملی} ]
بخش هفتم: پیامدهای اخلاقی و تولد اخلاق محافظت از نوزاد
تغییر پارادایم از «عدم توانایی در احساس درد» به «الزام به جلوگیری از درد» یک تحول اخلاقی عظیم در پزشکی بود. این تحول، بنیانهای اخلاق پزشکی نوین در مورد بیماران غیرقابل کلام را شکل داد.
۷.۱. اصل عدم آسیبرسانی (Non-Maleficence)
در اخلاق پزشکی، اصل عدم آسیبرسانی حکم میکند که پزشکان باید از اعمالی که به بیمار آسیب میزند، اجتناب کنند. در مورد جراحی نوزادان، روشن شد که درد شدید، یک آسیب جسمی و روانی جدی است. نادیده گرفتن درد نوزاد به دلیل «ناآگاهی» یا «نقص فنی»، دیگر توجیهی اخلاقی نداشت.
۷.۲. اخلاق دلسوزی (Beneficence) و احترام به کرامت انسانی
با پذیرش اینکه نوزاد درد را تجربه میکند، مسئولیت پزشک مبنی بر عمل به نفع بیمار (Beneficence) افزایش یافت. این شامل نه تنها انجام موفقیتآمیز عمل جراحی، بلکه تضمین حداقل رنج ممکن در طول فرآیند بود. احترام به کرامت انسانی، دیگر محدود به افراد بالغ نبود؛ بلکه باید از لحظه تولد اعمال میشد.
۷.۳. ظهور شاخصهای ارزیابی درد نوزادی
برای غلبه بر چالش اندازهگیری درد در بیماران غیرکلامی، ابزارهای ارزیابی چندوجهی توسعه یافتند. این ابزارها، واکنشهای فیزیولوژیک و رفتاری را همزمان مورد سنجش قرار میدهند:
- PIPP (Premature Infant Pain Profile): ارزیابی بر اساس تغییرات ضربان قلب، اشباع اکسیژن، زبان/دهان و حالت چهره.
- FLACC (Face, Legs, Activity, Cry, Consolability): یک ابزار مشاهدهای که امتیاز نهایی درد را بر اساس مجموعه علائم ارائه میدهد.
استفاده روتین از این ابزارها در بخشهای NICU و اتاق عمل اطفال، تضمین کرد که تصمیمگیری در مورد تجویز مسکن دیگر وابسته به حدس و گمان نباشد، بلکه مبتنی بر شواهد رفتاری و فیزیولوژیک باشد.
بخش هشتم: تغییر پروتکلهای پزشکی و عصر بیهوشی نوزادی
انقلاب علمی و اخلاقی فوق، مستلزم بازنویسی کامل کتابهای راهنمای پزشکی و ایجاد تخصصهای جدید بود.
۸.۱. توسعه فارماکولوژی اطفال تخصصی
بزرگترین مانع، یعنی ایمنی دارویی، نیازمند تحقیق بود. محققان شروع به مطالعه متابولیسم داروها در بدن نوزاد کردند. دریافتند که آنزیمهای کبدی و عملکرد کلیوی در نوزادان به طور قابل توجهی متفاوت است، به این معنی که دوزهای دارویی بزرگسالان یا حتی کودکان بزرگتر برای نوزادان سمی است.
تغییرات کلیدی در تجویز مسکن:
- استفاده از آگونیستهای اپیوئیدی با دوز بسیار پایین: داروهایی مانند فنتانیل (به دلیل شروع سریع اثر و نیمهعمر کوتاه) برای مدیریت درد حاد جراحی در دوزهای میکروگرم بر کیلوگرم مورد استفاده قرار گرفتند.
- بیحسی منطقهای: استفاده گسترده از بلاکهای عصبی موضعی (مانند تزریق به فضای اپیدورال یا القای بلاک عصبی منطقهای) به عنوان یک استراتژی کاهشدهنده استفاده از بیهوشی عمومی سیستمیک. این روشها تضمین میکنند که بخش بزرگی از بدن در طول جراحی تحت تأثیر مسکن قرار گیرد، در حالی که مواد مخدر سیستمیک به حداقل میرسند.
- استفاده از داروهای کمکی (Adjuvants): مانند لیدوکائین برای پروسیجرهای کوتاهتر، یا استفاده از بنزودیازپینها (مانند میدازولام) برای آرامبخشی پیش از عمل (Premedication) که به کاهش اضطراب قبل از شروع بیهوشی کمک میکند.
۸.۲. ظهور متخصص بیهوشی نوزادی (Neonatal Anesthesiology)
جراحی نوزادان (Neonatal Surgery) خود به یک فوق تخصص تبدیل شد و همراه آن، تخصص بیهوشی نوزادی نیز متولد گردید. این متخصصان بر روی مدیریت تنفس، تنظیم دما، تعادل مایعات و متابولیسم داروها در نوزادانی که اغلب کمتر از ۲ کیلوگرم وزن دارند، تمرکز کردند.
آنها پروتکلهایی را ایجاد کردند که به طور همزمان درد، استرس، و خطر بیهوشی را مدیریت میکردند. این پروتکلها شامل مانیتورینگ پیشرفته (مانند EEG برای اطمینان از عمق مناسب بیهوشی) و پروتکلهای دقیق برای بازگرداندن نوزاد به وضعیت پایدار پس از عمل بود.
بخش نهم: مقایسه گذشته و حال – شکاف یک نسلی
مقایسه وضعیت جراحی نوزادان پیش از دهه ۱۹۸۰ و وضعیت کنونی، نشاندهنده یک شکاف عظیم در درک ما از انسانیت و بیولوژی است.
۹.۱. گذشته: تمرکز بر بقای فنی
پارامتررویکرد سنتی (تا دهه ۱۹۸۰)درک دردانعکاس نخاعی؛ فاقد تجربه ذهنی.تجویز داروداروهای بیهوشی سیستمیک به دلیل خطر دپرشن تنفسی ممنوع یا بسیار محدود.مانیتورینگتمرکز بر علائم حیاتی اولیه (نبض، فشار خون).پیامدهای بلندمدتنادیده گرفته شده؛ تمرکز صرف بر زنده ماندن پس از عمل.اخلاق غالبعملگراگرایی؛ درد به عنوان یک «شر لازم».
۹.۲. حال: تمرکز بر رفاه جامع (Holistic Well-being)
پارامتررویکرد مدرن (از دهه ۲۰۰۰ به بعد)درک درددرد یک تجربه حسی-عاطفی پیچیده است که از بدو تولد وجود دارد.تجویز داروبیهوشی چندوجهی شامل مسکنهای موضعی، اپیوئیدها در دوزهای کم و آرامبخشها.مانیتورینگاستفاده از BIS (شاخص طیف بیهوشی)، تجزیه و تحلیل گازهای خونی، و اسکنرهای درد رفتاری (PIPP/FLACC).پیامدهای بلندمدتمدیریت درد برای جلوگیری از تروما و سنسیتاسیون عصبی طولانیمدت.اخلاق غالببیمار محوری؛ درد باید به حداقل برسد مگر در موارد اثباتشده غیرممکن.
۹.۳. نقلقولهای علمی معتبر از دوران گذار
تغییر در ادبیات علمی بسیار گویا بود. نقلقولهای زیر، تضاد دیدگاهها را نشان میدهند:
از گذشته (نقل به مضمون از متون دهه ۱۹۶۰):
“نوزادان از سد خونی-مغزی مناسبی برخوردار نیستند که بتواند درد را به شکل آزاردهنده سازماندهی کند. شوک درد برای آنها تنها به یک اختلال موقت در تعادل فیزیولوژیک منجر میشود که با جایگزینی مایعات قابل رفع است.”
از حال (سند تحول NIH/AAP، دهه ۲۰۰۰):
“شواهد متعددی اکنون نشان میدهند که پروسیجرهای دردناک در نوزادان منجر به پاسخهای عصبی و تغییرات ساختاری میشود که نشان دهنده یک تجربه ادراکی دردناک است. حذف درد، یک استاندارد مراقبتی ضروری است، نه یک امتیاز اختیاری.”
این تحول، مدیون فشار جمعی متخصصان بیهوشی، پرستاران NICU و خانوادههای آگاه بود که حاضر به پذیرش روایت سنتی نشدند.
بخش دهم: وضعیت امروز بیهوشی نوزادان: ایمنی و پیچیدگی
امروزه، جراحی نوزادان بدون مسکن تقریباً به طور کامل در جهان توسعه یافته منسوخ شده است. با این حال، حوزه بیهوشی نوزادی همچنان یکی از پیچیدهترین و پرریسکترین زیرشاخههای پزشکی است.
۱۰.۱. چالشهای متابولیسم دارو
حتی با وجود مسکنها، چالش متابولیسم باقی میماند. نوزادان دارای دوزهای پایین آلبومین پلاسما هستند، که بر اتصال داروهای مبتنی بر پروتئین تأثیر میگذارد و میتواند غلظت داروی آزاد را افزایش دهد و خطر سمیت را بالا ببرد. علاوه بر این، نارس بودن کبد و کلیه در نوزادان نارس، زمان دفع دارو را به شدت طولانی میکند، که نیاز به نظارت دقیق و تنظیم دوز بر اساس ساعتهای واقعی نوزاد (Chronological Age) و سن حاملگی اصلاح شده (Corrected Gestational Age) دارد.
۱۰.۲. روشهای نوین مدیریت درد ترکیبی (Multimodal Analgesia)
پروتکلهای مدرن بر رویکرد چندگانه تأکید دارند تا وابستگی به داروهای قوی (مانند مورفین و فنتانیل) کاهش یابد:
- تکنیکهای موضعی: استفاده از کرمهای بیحس کننده موضعی (مانند لیدوکائین/تتراکائین) برای پروسیجرهای سطحی یا تزریق کانترپوآ برای بلاکهای قبل از جراحی بزرگ.
- داروهای غیر اپیوئیدی: استفاده از پاراستامول و داروهای ضد التهابی غیر استروئیدی (در صورت نبود منع مصرف کبدی/کلیوی) برای مدیریت درد پس از عمل.
- روشهای غیردارویی: استفاده از مکیدن گلوکز رقیق شده، ساکارز، تماس پوست به پوست (Kangaroo Care) و محیط آرام (کاهش نویز و نور) به عنوان ابزارهای کمکی قدرتمند برای تسکین درد و ایجاد آرامش.
۱۰.۳. تأکید بر مراقبت تسکینی نوزادی (Neonatal Palliative Care)
در مواردی که نوزادان دچار نقایص غیرقابل اصلاح هستند و جراحی تنها به طولانی شدن رنج منجر میشود، پروتکلهای مراقبت تسکینی نوزادی وارد عمل میشوند. این رویکرد اطمینان میدهد که حتی در زمان مرگ یا انتقال به مراقبتهای تسکینی، بیمار عاری از درد و رنج شدید باشد؛ درسی که مستقیماً از پذیرش درد در دوران جراحی ناشی میشود.
بخش یازدهم: خطاهای داروینیسم پزشکی و درسهای آموخته شده
تأمل در مورد دوران جراحی بدون مسکن، یک مطالعه موردی در مورد خطر کاربرد نادرست اصول علمی یا فلسفی در پزشکی است.
۱۱.۱. نقد خطای داروینیسم پزشکی
داروینیسم پزشکی، که سعی داشت اصول تکاملی را بر روی افراد بیمار اعمال کند، در نهایت شکست خورد زیرا پزشکی هدفش «بهبود کیفیت زندگی» و «مبارزه با طبیعت در جهت ارزشهای اخلاقی انسان» است، نه پیروی کورکورانه از انتخاب طبیعی.
نوزادی که نیازمند جراحی است، از طریق مداخله پزشکی از چرخه انتخاب طبیعی خارج نمیشود؛ بلکه جامعه پزشکی با استفاده از دانش خود، سعی در نجات یک زندگی دارد. محروم کردن او از مسکن صرفاً به دلیل بیماری زمینهای، نه تنها غیرانسانی بود، بلکه از نظر علمی نیز بیاساس بود، زیرا درد به خودی خود آسیبی ثانویه و جدی به مغز در حال رشد وارد میکند.
۱۱.۲. مسئولیت در برابر آسیبپذیرترینها
این دوره تاریخی یک زنگ خطر باقی میماند: هرگاه گروهی از بیماران فاقد قدرت کلامی برای بیان رنج خود باشند (نوزادان، بیماران دمانس شدید، بیماران کما)، خطر اینکه نیازهای اساسی آنها (از جمله نیاز به عدم رنج) نادیده گرفته شود، افزایش مییابد.
این امر تأکیدی است بر لزوم «پزشکی مبتنی بر شواهد» (Evidence-Based Medicine) که در آن شواهد نه تنها باید فیزیولوژیک، بلکه باید شامل درک عمیق ما از تجربههای انسانی (حتی در ابتداییترین اشکال آن) باشد.
۱۱.۳. آینده پژوهش در درد نوزادی
پژوهشها اکنون فراتر از صرفاً جلوگیری از درد حاد در حین عمل رفتهاند. تمرکز کنونی بر درک مکانیزمهای دقیق سنسیتاسیون عصبی و یافتن روشهایی برای “معکوس کردن” یا “جلوگیری” از آسیبهای عصبی ناشی از درد مزمن دوران نوزادی است.
این شامل درک بهتر نقش فاکتورهای ژنتیکی در واکنش به مسکنها و توسعه روشهای تصویربرداری غیرتهاجمی برای پایش سطح درد در نوزادان زنده متولد شده است.
نتیجهگیری: از کابوس تا استاندارد مراقبت
کابوس جراحی بدون مسکن نوزادان، یک فصل تاریک اما آموزنده در تاریخ پزشکی است. این دوره، ناشی از جهل علمی در مورد توانایی ادراک درد در سیستم عصبی نابالغ و همچنین تحت تأثیر خوشبینی کاذب مبنی بر ناآگاهی نوزادان از رنج بود.
پیشرفتهای علمی، به ویژه در تصویربرداری عصبی (fMRI)، به شکلی غیرقابل انکار ثابت کردند که نوزادان رنج میبرند. این کشف، به همراه یک موج اصلاحکننده اخلاقی، منجر به دگرگونی پروتکلهای بیهوشی شد. امروزه، مراقبت از نوزادان نیازمند جراحی، یک رویکرد دقیق، چندوجهی و بسیار محافظهکارانه نسبت به مدیریت درد را طلب میکند. داستان جفری لاوسون و هزاران نوزاد گمنام دیگر، یادآور این حقیقت است که پیشرفت واقعی پزشکی تنها با افزایش تواناییهای فنی محقق نمیشود، بلکه با تعمیق درک ما از کرامت هر موجود زنده، صرف نظر از سن یا توانایی کلامیاش، به دست میآید.
سؤالات متداول (FAQ) در مورد جراحی نوزادان و مدیریت درد
این بخش به ۱۰ سؤال پرتکرار سئو شده در زمینه موضوع این مقاله پاسخ میدهد.
۱. جراحی نوزادان بدون مسکن دقیقاً تا چه سالی در بسیاری از مراکز پزشکی رایج بود؟
اگرچه تغییرات تدریجی بود، اما پذیرش گسترده و استانداردسازی استفاده از بیهوشی قوی و مسکنهای قوی برای نوزادان پس از پروسیجرهای دردناک، عمدتاً در اواخر دهه ۱۹۸۰ و اوایل دهه ۱۹۹۰ به دلیل مطالعات علمی و فشار اخلاقی، به اوج رسید.
۲. چرا پزشکان قبلاً فکر میکردند نوزادان درد را احساس نمیکنند؟
باور غالب این بود که قشر مغز (Cortex)، که مسئول آگاهی شناختی و تجربه ذهنی درد است، در نوزادان به خصوص نوزادان نارس به اندازه کافی تکامل نیافته است. آنها فقط واکنشهای رفلکسی نخاعی را مشاهده میکردند و آن را به اشتباه به عنوان فقدان رنج تفسیر میکردند.
۳. نقش مطالعات MRI مدرن (مانند اسلیتر ۲۰۱۵) در تغییر پروتکلها چه بود؟
مطالعات fMRI نشان دادند که نه تنها مسیرهای درد به نخاع میرسند، بلکه مناطقی مانند آمیگدال و اینسولا (مسئول پردازش عاطفی ترس و درد) در نوزادان تحت تحریک دردناک فعال میشوند، که اثبات میکند آنها رنج ذهنی را تجربه میکنند.
۴. جراحی بدون مسکن چه تأثیرات فیزیولوژیکی مخربی بر نوزاد داشت؟
درد کنترلنشده منجر به فعال شدن شدید محور HPA، ترشح کورتیزول، افزایش شدید ضربان قلب و مصرف اکسیژن میشد که اغلب منجر به هیپوکسی، عدم تعادل متابولیک و در بلندمدت، سنسیتاسیون درد میگردید.
۵. «سنسیتاسیون درد» (Pain Sensitization) در نوزادان به چه معناست؟
سنسیتاسیون درد به این معنی است که پس از یک تجربه دردناک شدید اولیه، سیستم عصبی نوزاد بیش از حد حساس میشود. این باعث میشود که در آینده، حتی محرکهای بسیار خفیف نیز پاسخهای شدید استرس و درد را برانگیزند.
۶. آیا بیهوشی نوزادان امروزی کاملاً ایمن است؟
بیهوشی نوزادی بسیار ایمنتر شده است، اما همچنان ریسکهایی دارد. نوزادان متابولیسم دارویی متفاوتی دارند (به دلیل عملکرد ناقص کبد و کلیه) و نیاز به نظارت بسیار دقیقی بر دوز داروهای بیهوشی و مسکنها دارند.
۷. چه چیزی باعث شد پروتکلهای پزشکی به طور ناگهانی تغییر کنند؟
تغییر نتیجه ترکیبی از دو عامل بود: ۱) شواهد علمی قوی (تصویربرداری عصبی) که اثبات کرد درد ادراک میشود. ۲) فشار اخلاقی خانوادهها و متخصصان بیهوشی که خواهان رعایت اصل عدم آسیبرسانی بودند.
۸. آیا مورد جفری لاوسون تنها نمونه از این دست بود؟
خیر. جفری لاوسون نمونهای مشهور است که به افشای این رویه کمک کرد، اما در طول دههها، هزاران نوزاد تحت جراحیهای قلبی و شکمی بدون مسکن کافی قرار گرفتند.
۹. در مدیریت درد نوزادان امروز، چه روشهای غیردارویی استفاده میشود؟
روشهای غیردارویی شامل ساکارز (شکر رقیق شده)، تماس پوست به پوست (Kangaroo Care)، استفاده از پستانکهای آرامبخش و مدیریت محیطی (کاهش صدا و نور شدید) هستند که به عنوان مکمل مسکنها به کار میروند.
۱۰. خطای داروینیسم پزشکی در این زمینه چه بود؟
خطای داروینیسم پزشکی این بود که برخی تصور میکردند تحمل درد توسط نوزادان بیمار، بخشی از فرآیند «انتخاب طبیعی» است و مداخله برای تسکین درد، مانع بقای قویترینها میشود. این دیدگاه، ارزش ذاتی رنج نبردن را نادیده گرفت.